神経内科学
本邦における神経内科学の芽生えは1902年に遡りますが、医療法としての診療科として「神経内科」の標榜が定められたのは1975年と新しい診療領域です。しかし、高齢化とともにその領域の社会的なニーズが高まっています。網羅する疾患は、脳血管障害、認知症、神経変性疾患(パーキンソン病、筋萎縮性側索硬化症、脊髄小脳変性症など)、神経免疫性疾患(多発性硬化症、重症筋無力症など)、てんかん、片頭痛など、多彩です。いずれもその診断、治療に高度の専門性を要求される領域ですが、地域医療における神経内科専門医はまだまだ不足しています。関西における臨床神経学の拠点として、一人でも多くの優れた専門医を輩出することを教室の使命と考えています。
脳を知り、脳を守る:Neuroscienceに基づいた病態解明と、より良い治療を
本学の神経内科学講座は平成9年(1997年)の創設された比較的新しい教室ですが、臨床講座としての体制およびスタッフが充実するとともに、現在では(1)脳血管障害(脳微細血管障害の病態解明、脳血管内治療の臨床研究)、(2)神経免疫疾患(多発性硬化症などの病態解明および治療法)、(3)神経変性疾患(大脳基底核神経回路可塑性、神経変性疾患の病理学的研究)と大きく3つに分けた研究活動を展開しています。臨床とニューロサイエンスに根ざした研究を展開し、多くの臨床応用に繋がることを目指しています。
現在の研究のテーマ
1. 脳血管障害
a) 脳微細血管障害の病態解明(薬師寺)
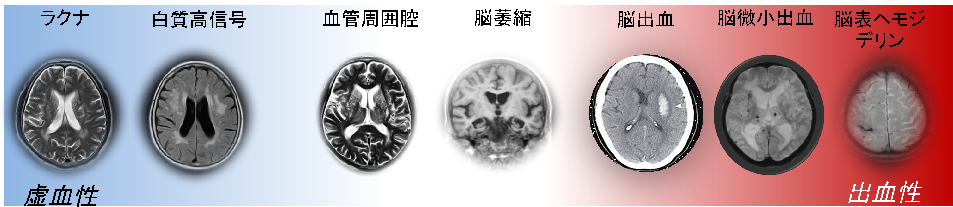
脳内の1mmに満たない微細血管障害は「脳小血管病(Cerebral small vessel disease: SVD)」と呼ばれます。これらの障害は現在の画像装置をもっても直接確認することはできず、脳MRIに出現する付随病変(図)でその分布・程度を把握することができます。近年の私達の取り組みとしては、高血圧性SVDが白人に比べ日本人に多いこと(Neurology 2019; J Neurol Sci 2020)、前述の付随病変に基づいたSVD重症度スコア(Summary SVD Score)が脳梗塞再発に関与すること(Front Aging Neurosci 2023)、スコアの経時的悪化には中年期の血圧値・喫煙が関与することを報告しました。今後は脳アミロイド血管症の発症メカニズムに関する検討も深めていき、SVD領域における本邦のトップランナーを目指します。
b) 頸動脈ステント留置術後の過灌流に関する検討(國枝)
頸動脈ステント留置術(CAS)後の過灌流(CHP)は重篤な周術期合併症を引き起こし得るため、その発生の予測と予防治療の確立が期待されています。CHPの予測に関しては、近年SPECTで算出された脳循環予備能(CVR)低下がCHPと関連しているとの報告が散見されています。そこで、われわれはSPECTで算出されたCVRと脳血管造影検査の所見を比較し、leptomeningeal collaterals(LM)の存在がCVR 低下と強く関連していることを報告しました(Intern Med. 2017)。この結果は、LMの存在がCHPと関連している可能性を示唆しており、CASの周術期管理に有用と考えられました。また、CHPの発生予防に関しては、現在まで確立した治療は存在しないため、われわれは、フリーラジカルスカベンジャーであるedaravoneをCAS術前に投与し、CAS後のCHP発生予防に効果があるか否かのランダム化比較試験(RCT)を行いました。結果、edaravone術前投与のCHP発症抑制効果を示すことはできませんでした(Interdiscip Neurosurg. 2021)。そこで、現在は酸化ストレスマーカーの一つである尿中8-OHdGをCAS周術期に測定することで、CASにおけるフリーラジカルの変化動態を明らかにする取り組みを行っています。
c) 脳アミロイドアンギオパチーの病態解明(村上)
脳アミロイドアンギオパチー(CAA)は、60歳以上の約50%で認められ高齢者の脳出血の主要な原因となります。CAAは再発が多く、難治性ですが確立した治療法がありません。そこで私たちは、神経細胞および血管の保護作用が示されている神経栄養因子であるニューレグリン-1(NRG1)/ErbBシグナルに着目し、CAAの病態解明を目的とし研究を進めています。ErbB受容体は、NRG1などのリガンド刺激により二量体化・リン酸化し、Ras-MAPKやPI3K-Akt 経路を活性化させます。これにより、増殖・分化・細胞死などの多様な細胞応答が誘導されます。さらに、NRG1/ErbBシグナルが様々な神経変性疾患に関与している可能性も報告されています(Neuropathol Appl Neurobiol. 2018)。私たちは、CAA剖検脳を用いたNRG1/ErbBシグナルの解析、およびCAAモデルマウスに対するNRG1の投与を行い、NRG1がCAA重症度や血管破綻に与える影響とその下流シグナルの変化を明らかにし、病態解明や治療法の開発を目指します。
2. 神経免疫疾患
免疫性神経疾患に対する臨床および基礎研究(近藤)
a) 多発性硬化症(MS)疾患修飾薬への治療不応性を予見する臨床所見、神経画像所見について解析を進めています(Front Neurol, 2021)。今後はMRIの中心静脈サインを持つ病巣頻度と治療反応性の解析を進めます。また、免疫細胞の産生するサイトカインプロフィルと疾患修飾薬治療反応性が相関するかどうかを解析しています(Front Neurol, 2022)。
b) 多発性硬化症や視神経脊髄炎の免疫学的背景に関して、T細胞性免疫応答を中心に解析しています(Neurol Neuroimmunol Neuroinflamm, 2023)。神経免疫疾患の治療薬として抗補体薬が使用されるようになりました。T細胞上C5a受容体の刺激がT細胞の活性化、産生サイトカインプロファイルに与える影響が、神経免疫疾患の免疫病態にどう関わるかを解析予定です。
c) ミエリン糖脂質スルファチドの免疫細胞活性化への影響を解析しています。現在までに、スルファチドがT細胞の増殖抑制をさまざまな機序で抑制すること、しかし、進行期のMSではスルファチドのT細胞増殖抑制効果が減弱していることを明らかにしています(Mol Neurobiol, 2022)。一方、B細胞に対しては凝集、抗体産生を促進することも観察しており、機序について解析を進めます。
d) 重症筋無力症(MG)のT細胞性免疫応答を解析しています。ICOSを強発現する濾胞性T細胞(CXCR5陽性)増加しており、その頻度は重症度は相関していることを明らかにしています(Neurol neuroimmunol neuroinflamm, 2021 ) 。
3. 神経変性疾患
a) パーキンソン病の病態解明(髙橋)
神経難病医学講座は2023.4月に関西医科大学で初めての寄附講座として設立されました。
京都大学関連病院と株式会社サンウェルズとの連携による「PDハウス」での臨床研究を開始し、高橋牧郎が責任者となり関西地区におけるパーキンソン病専門医ホーム「PDハウス」との診療、教育、研究における連携や、臨床研究より得られる知見の論文・学会発表を予定しており、医療、介護、看護の多職種介入による神経変性疾患の予後に与える影響を検討し、施設援助を拡充してまいります。
また、多職種介入による効果の評価やウェアラブルデバイスを用いた症状モニタリング、臨床試験の促進によって質の高いデータ解析性が可能になり、ここから得られた知見に基づいて、PD患者のADLおよびQOLを高める有効な介護施設および住居のハードおよびソフト面でのイノベーションにつながることが期待され、さらには、パーキンソン病療養指導士をはじめとする在宅介護領域におけるPDケアに特化した医療従事者の人材の育成も期待できます。
現在、e-sportsなどのソフトを用いたリハビリ介入がPDの諸症状に与える影響を解析し、臨床に役立てる研究を行うことを目指しています。
また、 進行期パーキンソン病に見られる薬効不安定(wearing off, dyskinesia)のある患者さんを対象に経皮的フォスレボドパ持続注入療法(ビアレブ)を積極的に導入し、その長期的効果、疾患修飾効果につき、解析を行なっています。
また、病理研究チームと共同でαシヌクレインをはじめとする病理・生化学的解析についても行っていく予定です。
b) 筋萎縮性側索硬化症の病態解明(中村)
筋萎縮性側索硬化症(ALS)は、全身の筋肉が急速に衰えてゆく神経疾患です。神経細胞には軸索輸送と呼ばれる高速輸送システムが存在します。キネシンファミリー1A(KIF1A)遺伝子のいくつかのバリアントは遺伝性痙性対麻痺を引き起こすことが報告されていますが、我々はKIF1A遺伝子の新規バリアントをALSで発見しました。このバリアントがKIF1Aの機能にどのような影響を及ぼしているのかを明らかにすることでALSの病態解明を目指します。
c) レビー小体病の病態解明(中村)
DNA損傷の中で最も重篤と考えられている二本鎖切断は、アルツハイマー病(AD)やパーキンソン病など多くの神経変性疾患の原因になっていると考えられています。近年、ADでは、アミロイドβがDNA損傷を誘導し、それに対してDNA損傷修復に関わるBRCA1の発現が増加しているものの、神経原線維変化内に蓄積していくことで、核内でのDNA修復ができず細胞傷害をきたしていることが報告されています。そこで今回シヌクレイノパチーでも同様にBRCA1によるDNA修復障害が起こっている可能性を考え、AD病理を伴うレビー小体病やAD病理を認めないレビー小体病とコントロールの剖検脳を用いて、シヌクレイノパチーの病態を解明することを目指しています。
研究業績
![[KMU BRAND]関西医科大学 関連施設](/common/img/logo_brand.png)